
引言
新年特輯 | 奧泰康2023年終盤點日邁月征,朝暮輪轉
2023 漸行漸遠
2024 悄然而至
過去一年
在日新月異的變革中
我們一同親歷了醫療行業的高速發展
與合作伙伴分享市場準入的喜悅
感恩大家一路的支持與陪伴
是團隊的力量推動每一個項目落地
最終見證了里程碑的達成
讓我們跟隨時間
共同回顧2023年一起走過的精彩旅程
1月
脊髓刺激系統-首例植入
 1月,脊髓刺激系統(SCS)臨床試驗在浙醫一院疼痛科順利完成首例臨床植入,產品用于慢性疼痛,臨床驗證工作將為產品未來在中國上市提供更全面的臨床依據.
1月,脊髓刺激系統(SCS)臨床試驗在浙醫一院疼痛科順利完成首例臨床植入,產品用于慢性疼痛,臨床驗證工作將為產品未來在中國上市提供更全面的臨床依據.
2月
助力冠脈產品獲證

2月,藥物涂層PTCA球囊擴張導管(國械注準20233030115)獲得NMPA批準上市,奧泰康承擔本項目臨床試驗服務,系2023年奧泰康助力獲得的首張三類醫療器械注冊證。
富春山會議-發表演講
 2月,富春山•中國醫藥生物技術行業年度報告會暨2022年中國醫藥生物技術十大進展發布會召開,奧泰康應邀出席會議,圍繞《再生醫學生物材料引導組織修復器官再造的應用和創新》發表主題報告。
2月,富春山•中國醫藥生物技術行業年度報告會暨2022年中國醫藥生物技術十大進展發布會召開,奧泰康應邀出席會議,圍繞《再生醫學生物材料引導組織修復器官再造的應用和創新》發表主題報告。
眼科創新產品-全球首例植入
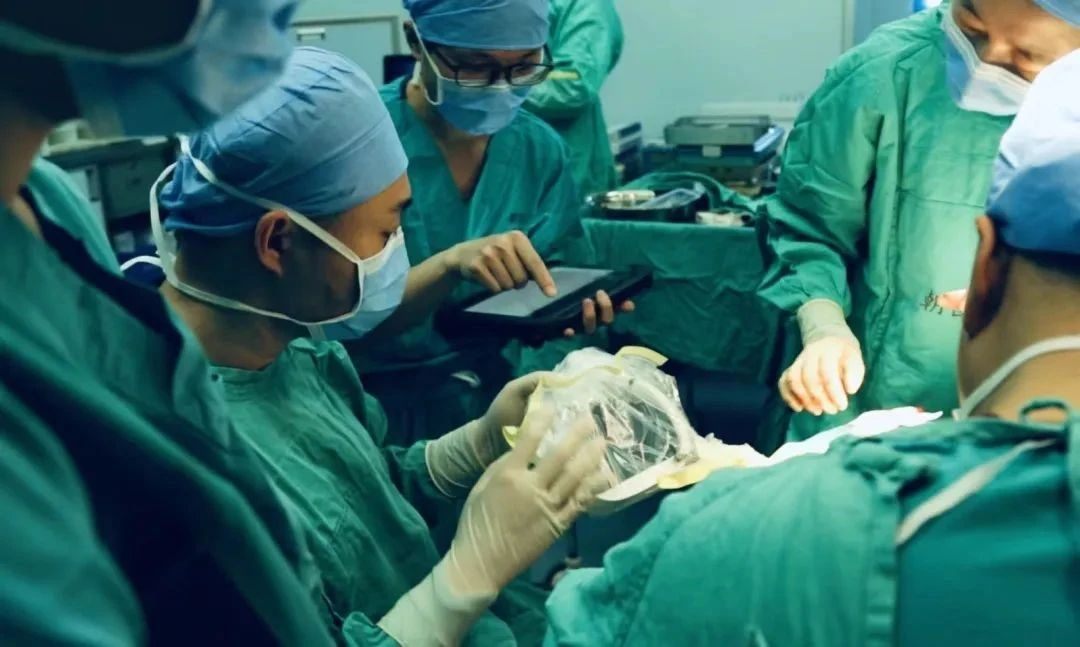 2月,植入式眼部肌肉神經刺激器i-NYS,在首都醫科大學附屬北京朝陽醫院完成全球首例植入,產品系全球首創且唯一用于治療先天性眼球震顫的三類有源植入式醫療器械,有望徹底破解眼球震顫的治療難題。
2月,植入式眼部肌肉神經刺激器i-NYS,在首都醫科大學附屬北京朝陽醫院完成全球首例植入,產品系全球首創且唯一用于治療先天性眼球震顫的三類有源植入式醫療器械,有望徹底破解眼球震顫的治療難題。
3月
介入二尖瓣腱索修復系統-臨床試驗啟動

3月,介入二尖瓣腱索修復系統臨床試驗正式啟動,并完成全國首例臨床應用,手術的圓滿完成讓團隊突破了外科手術局限,為試驗的進一步開展奠定信心和經驗基礎,全國多中心臨床試驗患者入組正式開始。
CIMDR-出席并發表演講
 3月,第十三屆中國醫療器械監督管理國際會議(CIMDR)落幕,奧泰康應邀出席會議,并在醫療器械創新分會中以《創新醫療器械研發設計與注冊》為主題進行分享,為醫療器械從業者帶來滿滿干貨,吸引眾多業內醫療同仁切磋交流.
3月,第十三屆中國醫療器械監督管理國際會議(CIMDR)落幕,奧泰康應邀出席會議,并在醫療器械創新分會中以《創新醫療器械研發設計與注冊》為主題進行分享,為醫療器械從業者帶來滿滿干貨,吸引眾多業內醫療同仁切磋交流.
助力心血管產品獲證
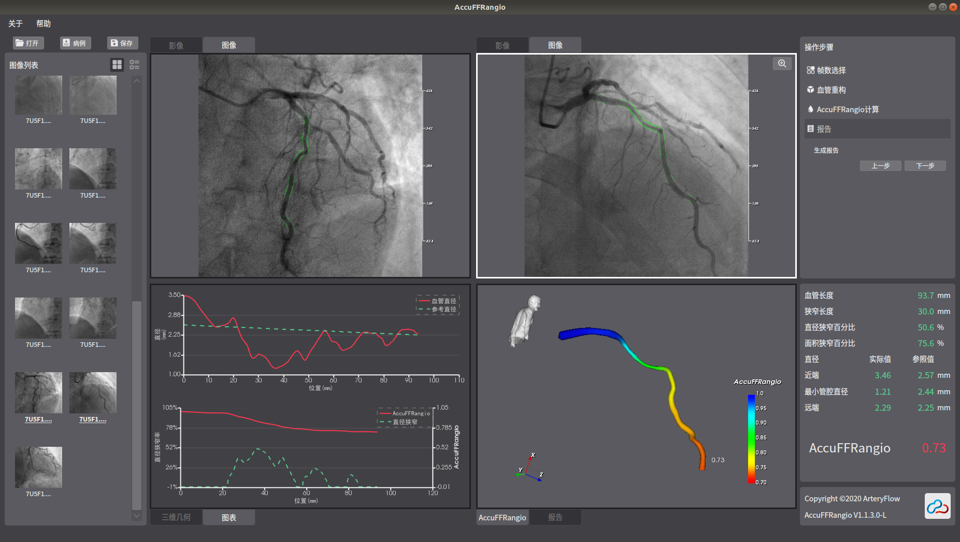 3月,冠脈造影血流儲備分數計算設備(國械注準20233070251)獲得NMPA批準上市,奧泰康承擔本項目臨床試驗服務,系2023年奧泰康助力獲得的第五張三類醫療器械注冊證。
3月,冠脈造影血流儲備分數計算設備(國械注準20233070251)獲得NMPA批準上市,奧泰康承擔本項目臨床試驗服務,系2023年奧泰康助力獲得的第五張三類醫療器械注冊證。
蘇州CDMO入圍吳中區合同成交額十強
 3月,奧泰康蘇州CDMO中心——蘇州蘇豪生物材料科技有限公司獲得吳中區2022年度技術合同成交額十強企業榮譽,未來奧泰康蘇州CDMO中心將立足再生醫學生物材料更好地發揮示范引領作用,持續推動安全、有效和質量可控的產品進入市場。
3月,奧泰康蘇州CDMO中心——蘇州蘇豪生物材料科技有限公司獲得吳中區2022年度技術合同成交額十強企業榮譽,未來奧泰康蘇州CDMO中心將立足再生醫學生物材料更好地發揮示范引領作用,持續推動安全、有效和質量可控的產品進入市場。
4月
助力FFR軟件獲證
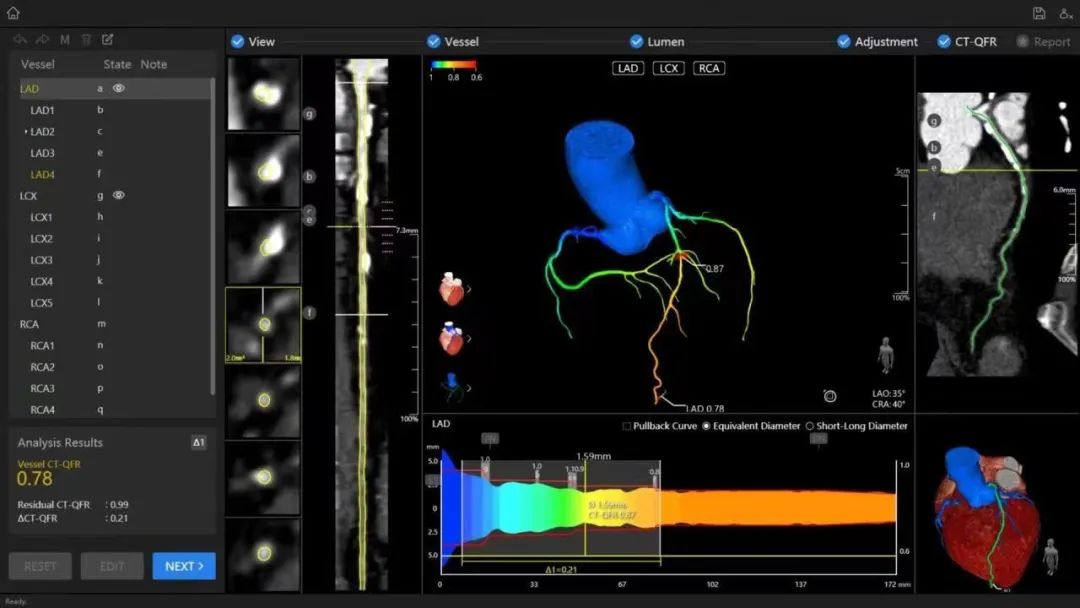 4月,冠狀動脈CT血流儲備分數計算軟件(國械注準20233210450)獲得NMPA批準上市,奧泰康承擔本項目臨床試驗服務,系2023年奧泰康助力獲得的第六張三類醫療器械注冊證。
4月,冠狀動脈CT血流儲備分數計算軟件(國械注準20233210450)獲得NMPA批準上市,奧泰康承擔本項目臨床試驗服務,系2023年奧泰康助力獲得的第六張三類醫療器械注冊證。
參加動脈網VB100 Mini論壇
 4月,由動脈網、VB100、蛋殼研究院、君聯資本等單位主辦的2023 VB100 Mini論壇中,奧泰康副總裁王成珍女士應邀出席活動,與眾多產業企業、投資機構的嘉賓,就產品從立項、設計、生產到臨床上市等全流程的關鍵要點展開深入探討。
4月,由動脈網、VB100、蛋殼研究院、君聯資本等單位主辦的2023 VB100 Mini論壇中,奧泰康副總裁王成珍女士應邀出席活動,與眾多產業企業、投資機構的嘉賓,就產品從立項、設計、生產到臨床上市等全流程的關鍵要點展開深入探討。
助力肺部AI產品獲證
 4月,肺結節CT圖像輔助檢測軟件(國械注準20233210530)獲得NMPA批準上市,奧泰康承擔本項目臨床試驗服務,系2023年奧泰康助力獲得的第7張三類醫療器械注冊證,也是公司累計助力獲得的第12張人工智能(AI)醫療器械注冊證
4月,肺結節CT圖像輔助檢測軟件(國械注準20233210530)獲得NMPA批準上市,奧泰康承擔本項目臨床試驗服務,系2023年奧泰康助力獲得的第7張三類醫療器械注冊證,也是公司累計助力獲得的第12張人工智能(AI)醫療器械注冊證
5月
國內器械CDMO平臺首張三類證獲批
 5月,奧泰康北京CDMO中心取得國家藥監局批準的三類醫療器械注冊證(國械注準20233140615),系全國首個以細胞外基質來源的膠原蛋白為原料制備的三類膠原貼敷料,也是器械CRO/CDMO行業受托研發誕生的全國首個三類醫療器械注冊證,具有里程碑意義。
5月,奧泰康北京CDMO中心取得國家藥監局批準的三類醫療器械注冊證(國械注準20233140615),系全國首個以細胞外基質來源的膠原蛋白為原料制備的三類膠原貼敷料,也是器械CRO/CDMO行業受托研發誕生的全國首個三類醫療器械注冊證,具有里程碑意義。
助力口腔產品獲證
 5月,骨填充材料(國械注準20233170649)獲得NMPA批準上市,奧泰康承擔本產品臨床試驗服務,系本年度奧泰康合作項目獲得的第9張三類醫療器械注冊證。
5月,骨填充材料(國械注準20233170649)獲得NMPA批準上市,奧泰康承擔本產品臨床試驗服務,系本年度奧泰康合作項目獲得的第9張三類醫療器械注冊證。
參加宣武醫院GCP培訓
 5月,首都醫科大學宣武醫院發起的“GCP+倫理”培訓,奧泰康臨床注冊部總監受邀參加并圍繞器械注冊研究分享主題報告。通過臨床試驗機構、倫理委員會、循證醫學中心等各方聯動合作,培訓進一步提高了研究者臨床研究能力,為臨床研究項目高質量發展奠定了良好基礎。
5月,首都醫科大學宣武醫院發起的“GCP+倫理”培訓,奧泰康臨床注冊部總監受邀參加并圍繞器械注冊研究分享主題報告。通過臨床試驗機構、倫理委員會、循證醫學中心等各方聯動合作,培訓進一步提高了研究者臨床研究能力,為臨床研究項目高質量發展奠定了良好基礎。
TAVR產品完成全部臨床入組
 5月,經導管主動脈瓣膜置換產品Xcor™完成全部可行性+確證性臨床試驗的患者入組,為全球心血管臨床醫生提供了具有扎實產品設計和臨床證據的創新解決方案,為Xcor™瓣膜不遠的將來完成產品注冊和全國推廣邁出了關鍵的一步。
5月,經導管主動脈瓣膜置換產品Xcor™完成全部可行性+確證性臨床試驗的患者入組,為全球心血管臨床醫生提供了具有扎實產品設計和臨床證據的創新解決方案,為Xcor™瓣膜不遠的將來完成產品注冊和全國推廣邁出了關鍵的一步。
應邀出席-中關村論壇

5月,奧泰康應邀出席2023中關村論壇國際技術交易大會,立足創新醫療器械和高端醫療器械,為企業參會代表展示研究開發、產品檢測、動物實驗、臨床試驗和產品注冊全流程解決方案,圍繞CRO&CDMO一體化服務進行答疑和交流,受到與會代表的肯定。
6月
沖擊波球囊導管系統-臨床首例入組
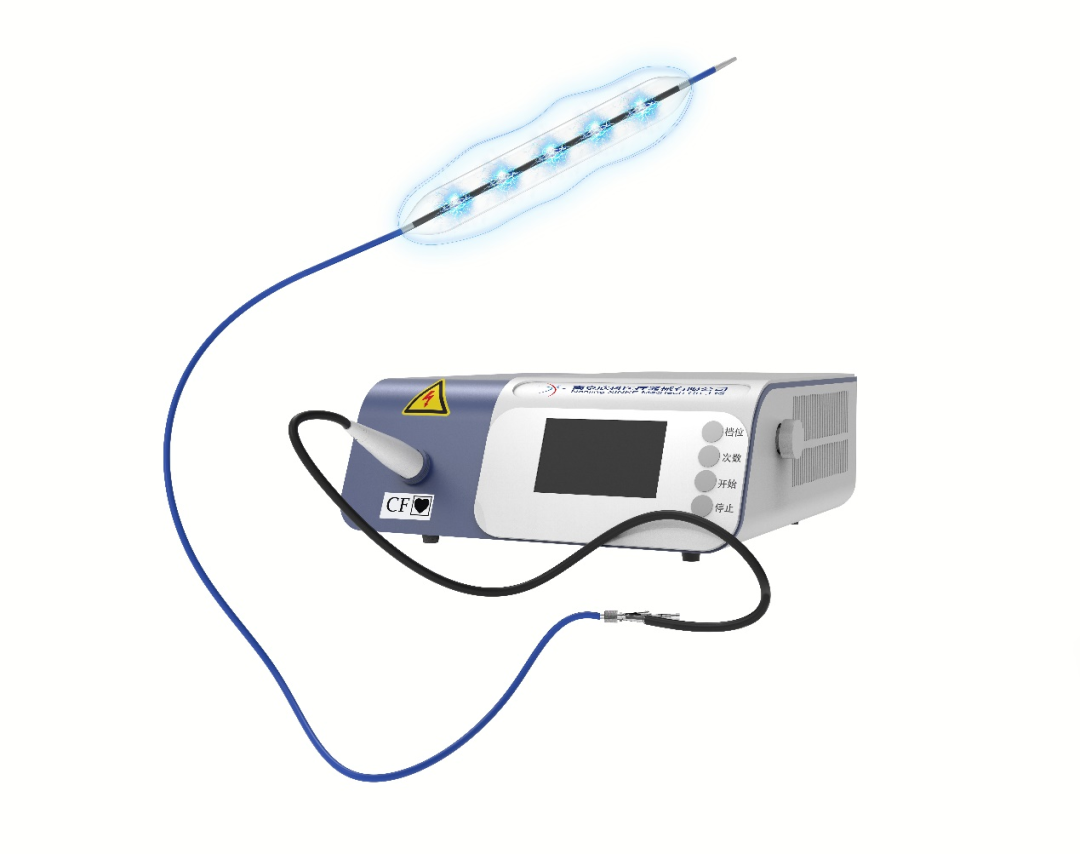 6月,外周血管內沖擊波球囊導管系統,上市前臨床研究完成首例患者入組,奧泰康負責臨床試驗服務,期待這一創新器械早日上市,為血管介入醫生提供新的鈣化病變治療選擇,造福廣大下肢動脈閉塞癥患者。
6月,外周血管內沖擊波球囊導管系統,上市前臨床研究完成首例患者入組,奧泰康負責臨床試驗服務,期待這一創新器械早日上市,為血管介入醫生提供新的鈣化病變治療選擇,造福廣大下肢動脈閉塞癥患者。
植發機器人-臨床試驗啟動會
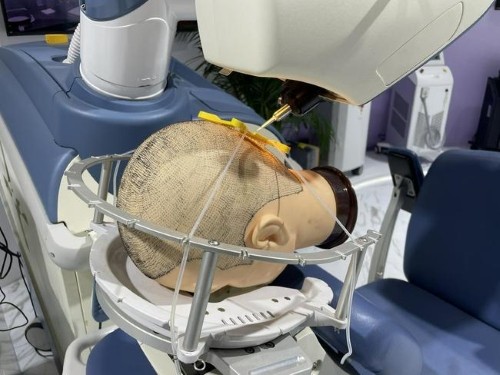
6月,植發機器人臨床試驗召開項目啟動會,參會專家對這一創新產品給予高度肯定,奧泰康作為臨床試驗服務方,也期待這一款產品今后能對國內植發行業帶來里程碑式升級。
通過創新型中小企業認定
 6月,奧泰康入選豐臺區2023年度第五批創新型中小企業名單,創新型中小企業的認定是國家根據企業創新能力、成長性、專業化三類指標評出,創新型中小企業一般包括技術創新、管理創新、市場敏感度、快速發展、貢獻就業、推動經濟等特點。
6月,奧泰康入選豐臺區2023年度第五批創新型中小企業名單,創新型中小企業的認定是國家根據企業創新能力、成長性、專業化三類指標評出,創新型中小企業一般包括技術創新、管理創新、市場敏感度、快速發展、貢獻就業、推動經濟等特點。
7月
恩施州領導蒞臨考察
 7月,恩施州州委副書記、州長夏錫璠,副州長曾凡勝,州政府秘書長程飛一行蒞臨奧泰康北京總部考察調研,奧泰康期待借助自身CRO在醫藥科技成果轉化方面的豐富經驗與優勢,助力恩施州傳統中醫藥和硒產品的新藥科技成果轉化,實現優勢互補、資源共享、共同推動生物醫藥行業高質量發展。
7月,恩施州州委副書記、州長夏錫璠,副州長曾凡勝,州政府秘書長程飛一行蒞臨奧泰康北京總部考察調研,奧泰康期待借助自身CRO在醫藥科技成果轉化方面的豐富經驗與優勢,助力恩施州傳統中醫藥和硒產品的新藥科技成果轉化,實現優勢互補、資源共享、共同推動生物醫藥行業高質量發展。
作為唯一的CRO企業入選億歐AI報告
 7月,世界人工智能大會中,億歐發布的《2023中國人工智能醫學影像產品生命周期研究報告》中,奧泰康作為醫學影像賽道企業圖譜中唯一的CRO企業入選報告。在AI醫學影像產品的市場準入方面,奧泰康與眾多頭部AI企業合作,承擔70余項AI產品的臨床服務,累計助力合作企業獲得AI三類醫療器械注冊證14張。
7月,世界人工智能大會中,億歐發布的《2023中國人工智能醫學影像產品生命周期研究報告》中,奧泰康作為醫學影像賽道企業圖譜中唯一的CRO企業入選報告。在AI醫學影像產品的市場準入方面,奧泰康與眾多頭部AI企業合作,承擔70余項AI產品的臨床服務,累計助力合作企業獲得AI三類醫療器械注冊證14張。
三類膠原貼敷料亮相2023CSD
 7月,奧泰康助力全國首個以細胞外基質來源的膠原蛋白為原料制備的三類膠原貼敷料亮相第28屆全國皮膚性病學術年會,北京交通大學教授、生物材料與再生醫學研究專家、奧泰康AOBM首席科學家王海濱教授應邀參加會議。與會專家對恒安芙林“麗點®膠原貼敷料”的有效性和安全性給予充分肯定,并對ECM膠原貼敷料核心技術給予高度評價。
7月,奧泰康助力全國首個以細胞外基質來源的膠原蛋白為原料制備的三類膠原貼敷料亮相第28屆全國皮膚性病學術年會,北京交通大學教授、生物材料與再生醫學研究專家、奧泰康AOBM首席科學家王海濱教授應邀參加會議。與會專家對恒安芙林“麗點®膠原貼敷料”的有效性和安全性給予充分肯定,并對ECM膠原貼敷料核心技術給予高度評價。
ECM生物凝膠產品-完成全部臨床入組
 7月,細胞外基質(ECM)生物凝膠產品完成全部臨床試驗受試者入組。此產品是國內首個進入臨床的ECM醫美注射產品,也是最新一代天然再生類醫美填充材料走向應用的重要里程碑,為將來產品注冊和全國推廣邁出關鍵性一步。
7月,細胞外基質(ECM)生物凝膠產品完成全部臨床試驗受試者入組。此產品是國內首個進入臨床的ECM醫美注射產品,也是最新一代天然再生類醫美填充材料走向應用的重要里程碑,為將來產品注冊和全國推廣邁出關鍵性一步。
創新產品獲批上市-靜脈支架系統
 7月,經國家藥品監督管理局公示,Inno-Xmart靜脈支架系統(國械注準20233131034)獲得NMPA批準上市,奧泰康承擔本項目創新申報服務
7月,經國家藥品監督管理局公示,Inno-Xmart靜脈支架系統(國械注準20233131034)獲得NMPA批準上市,奧泰康承擔本項目創新申報服務
8月
北京CDMO中心獲得生產許可證
 8月,奧泰康北京CDMO中心成功獲得由北京市藥品監督管理局頒發的創面敷料三類生產許可證(京藥監械生產許20230053號),標志著北京CDMO中心已達到醫療器械產業化生產的法規要求,具備醫療器械生產條件并可以正式投產,對公司產業化進程具有重要里程碑式意義。
8月,奧泰康北京CDMO中心成功獲得由北京市藥品監督管理局頒發的創面敷料三類生產許可證(京藥監械生產許20230053號),標志著北京CDMO中心已達到醫療器械產業化生產的法規要求,具備醫療器械生產條件并可以正式投產,對公司產業化進程具有重要里程碑式意義。
助力有源產品獲證
 8月,超聲高頻集成手術設備(國械注準20233011251)獲得NMPA批準上市,奧泰康承擔本項目臨床評價資料撰寫服務,系奧泰康助力獲得本年度第14張三類醫療器械注冊證。
8月,超聲高頻集成手術設備(國械注準20233011251)獲得NMPA批準上市,奧泰康承擔本項目臨床評價資料撰寫服務,系奧泰康助力獲得本年度第14張三類醫療器械注冊證。
9月
臨床注冊部&項目運營中心臨床培訓
 9月,奧泰康2023年臨床注冊部及項目運營中心臨床培訓圓滿結束,干貨滿滿的培訓議程具有極強的指導性和實用性,充分開拓了臨床執行思路,促進了臨床管理者和執行者間的學習與交流,為進一步提高臨床試驗項目質量保駕護航。
9月,奧泰康2023年臨床注冊部及項目運營中心臨床培訓圓滿結束,干貨滿滿的培訓議程具有極強的指導性和實用性,充分開拓了臨床執行思路,促進了臨床管理者和執行者間的學習與交流,為進一步提高臨床試驗項目質量保駕護航。
奧泰康十七周年慶典暨頒獎晚會

9月,奧泰康十七周年慶典暨頒獎晚會隆重舉行,線上直播平臺同步分享盛況,十七載征程,見證了奧泰康以專業服務賦能醫療的堅定步伐,感恩一路陪伴的伙伴,見證和參與公司的成長,奧泰康將以專業服務賦能醫療,奮楫篤行,臻于至善。
全球首款用于阿茲海默癥早期診斷的AI軟件獲批
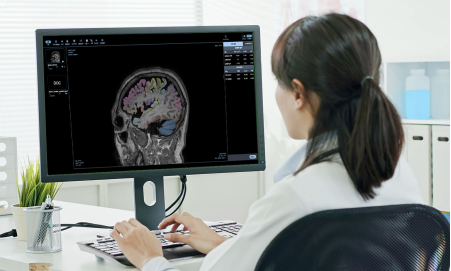
9月,磁共振圖像輔助評估軟件(國械注準20233211362)獲得NMPA批準上市,奧泰康承擔本項目臨床試驗服務,系2023年奧泰康助力獲得的第15張三類醫療器械注冊證,也是奧泰康累計助力獲得的第14張人工智能(AI)類醫療器械注冊證。
10月
應邀參加泰州醫博會

10月,奧泰康受邀參加第十四屆中國(泰州)國際醫藥博覽會,奧泰康CDMO中心在再生醫學生物材料領域深耕多年,積累豐富項目經驗及業內口碑,立足生物醫用材料市場準入全流程解決方案,向大眾展示了奧泰康醫療器械科技成果轉化一站式服務,受到眾多參會企業代表的肯定。
植入式眼部肌肉神經刺激器-完成全部臨床入組

10月,創新醫療器械“植入式眼部肌肉神經刺激器”(i-NYS)中國境內臨床試驗完成全部受試者入組,奧泰康承擔本項目臨床試驗服務,標志著由中國人自主研發制造的全球首款治療先天性眼球震顫的神經刺激器產品邁出了走向市場的堅實步伐,對于眼科領域“不治之癥”先天性眼球震顫的臨床治療具有突破性的里程碑意義。
奧泰康北京CDMO中心-喬遷儀式
 10月,奧泰康北京CDMO中心完成喬遷,研發生產車間規模進一步擴大,研發生產管線進行全面升級,廠房車間規模的擴大為企業發展奠定了堅實的基礎,為集團的未來注入了新的活力。奧泰康作為創新及高端醫療器械優質服務商入駐園區,將依托專業服務吸納更多專業化人才與科研力量,推動生物醫藥行業高質量發展。
10月,奧泰康北京CDMO中心完成喬遷,研發生產車間規模進一步擴大,研發生產管線進行全面升級,廠房車間規模的擴大為企業發展奠定了堅實的基礎,為集團的未來注入了新的活力。奧泰康作為創新及高端醫療器械優質服務商入駐園區,將依托專業服務吸納更多專業化人才與科研力量,推動生物醫藥行業高質量發展。
11月
助力外周產品通過創新審查
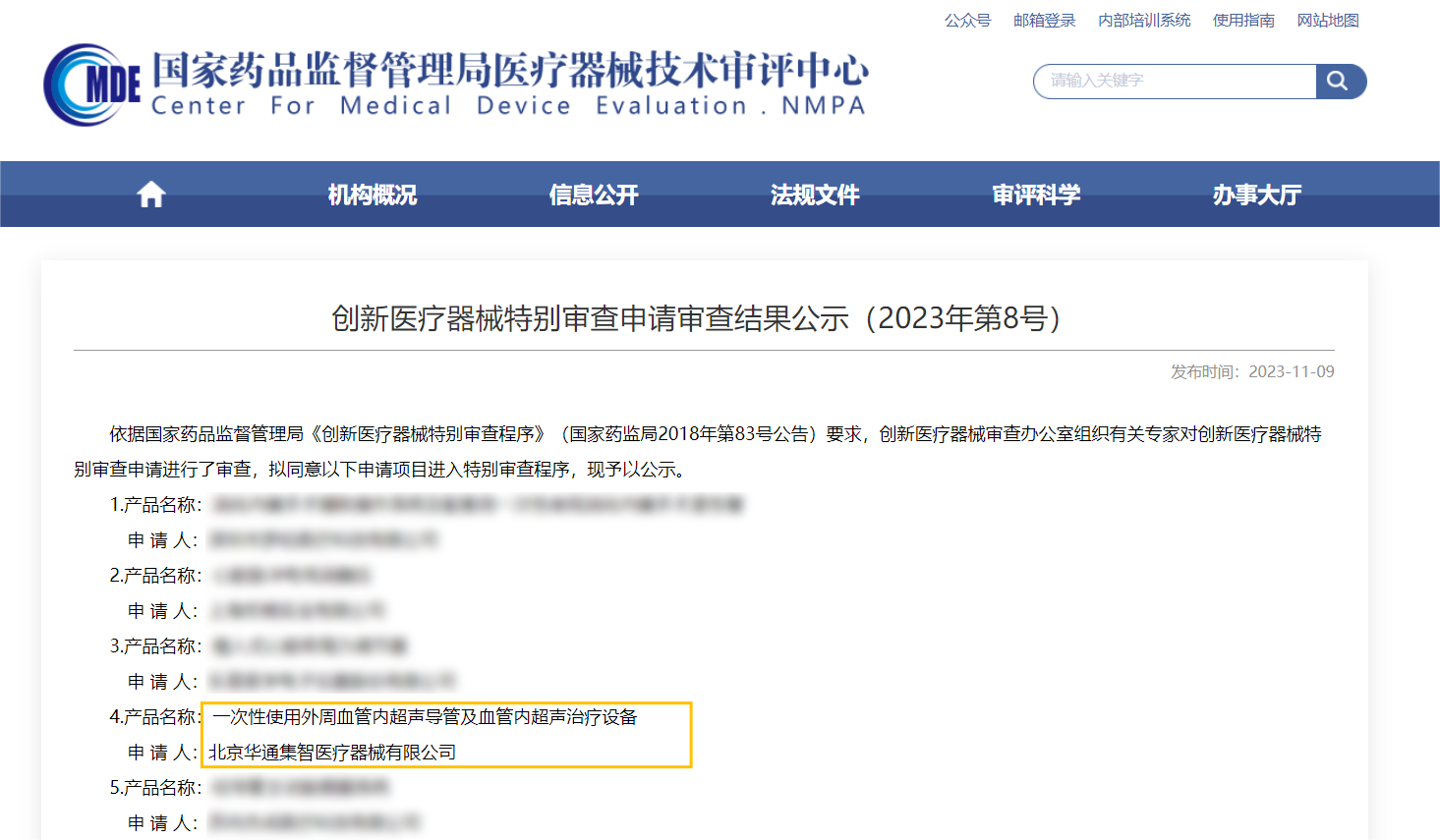
11月,一次性使用外周血管內超聲導管及血管內超聲治療設備通過創新醫療器械特別審查,奧泰康承擔本項目創新申報服務,截至目前,奧泰康已累計收獲19項創新申報成功案例。
助力FFR軟件獲批
 11月,冠狀動脈CT血流儲備分數計算軟件(國械注準20233211751)獲得NMPA批準上市,系國內唯一采用全三維流體力學+超級計算機原理的FFRCT產品,奧泰康承擔本項目注冊申報服務,系2023年奧泰康助力獲得的第17張三類醫療器械注冊證。
11月,冠狀動脈CT血流儲備分數計算軟件(國械注準20233211751)獲得NMPA批準上市,系國內唯一采用全三維流體力學+超級計算機原理的FFRCT產品,奧泰康承擔本項目注冊申報服務,系2023年奧泰康助力獲得的第17張三類醫療器械注冊證。
再生醫美項目-戰略合作簽約儀式
 11月,新氧科技與奧泰康舉行戰略合作簽約儀式,雙方開啟深層次合作新篇章。此次合作系奧泰康CRO&CDMO一體化服務的又一標志性事件,未來,奧泰康將充分發揮市場準入全流程解決方案服務優勢,推動再生醫美產品進入市場,實現醫美產品的全生命周期管理,為醫美行業高質量發展貢獻力量。
11月,新氧科技與奧泰康舉行戰略合作簽約儀式,雙方開啟深層次合作新篇章。此次合作系奧泰康CRO&CDMO一體化服務的又一標志性事件,未來,奧泰康將充分發揮市場準入全流程解決方案服務優勢,推動再生醫美產品進入市場,實現醫美產品的全生命周期管理,為醫美行業高質量發展貢獻力量。
12月
助力可吸收縫合線獲批
 12月,可吸收膠原蛋白縫合線(國械注準20233021868)獲得NMPA批準上市,奧泰康承擔本項目臨床試驗服務,系2023年奧泰康助力獲得的第18張三類醫療器械注冊證。
12月,可吸收膠原蛋白縫合線(國械注準20233021868)獲得NMPA批準上市,奧泰康承擔本項目臨床試驗服務,系2023年奧泰康助力獲得的第18張三類醫療器械注冊證。
凱歌而行,不以山海為遠
乘勢而上,不以日月為限
2023年度
奧泰康已累計助力21款產品獲批上市
未來,奧泰康將深耕CRO&CDMO服務
用實際行動達成更多的里程碑
行而不輟,未來可期
愿與您一路
奔赴嶄新的2024!